Kapasitas panas yang ada pada sebagian besar sistem tidaklah konstan,
namun bergantung pada variasi kondisi dari sistem termodinamika.
Kapasitas panas bergantung pada temperatur itu sendiri, dan juga tekanan
dan volume dari sistem.
Berbagai cara untuk mengukur kapasitas panas dapat dilakukan, yang secara umum dilakukan pada kondisi tekanankonstan atau volume konstan. Sehingga simbol kapasitas jenisnya disesuaikan, menjadi Cp untuk kapasitas jenis pada tekanan konstan, dan CV untuk
kapasitas jenis pada volume konstan. Gas dan cairan umumnya diukur pada
volume konstan. Pengukuran pada tekanan konstan akan menghasilkan nilai
yang lebih besar karena nilai tekanan konstan juga mencakup energi
panas yang digunakan untuk melakukan kerja untuk mengembangkan volume zat ketika temperatur ditingkatkan.
Panas jenis spesifik dari suatu zat merupakan molekul yang tidak pada
kondisi konstan melainkan bergantung pada temperaturnya. Temperatur pada
lingkungan pengukuran yang dibuat biasanya juga ditentukan. Conth dua
cara untuk menuliskan panas jenis dari suatu zat yaitu:
- Air (cair): cp = 4.1855 [J/(g·K)] (15 °C, 101.325 kPa) atau 1 kalori/gram °C
- Air (cair): CvH = 74.539 J/(mol·K) (25 °C)
Untuk cairan dan gas, penting untuk mengetahui tekanan yang digunakan
dalam menuliskan nilai kapasitas panas. Kebanyakan data yang
dipublikasikan dituliskan pada kondisi tekanan standar.
Hubungan termodinamika
Energi internal dari sebuah sistem tertutup akan berubah dengan menambahkan panas ke sistem atau ketika sistem melakukan kerja.

Untuk kerja sebagai hasil dari perubahan volume sistem:

Jika panas ditambahan pada volume konstan:

Jadilah kapasitas panas pada volume konstan, CV.
Untuk kapasitas panas pada tekanan konstan, CP, yang diturunkan dari persamaan perubahan entalpi:
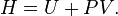
Perubahan pada entalpi dapat dirumuskan dengan:
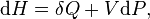
Sehingga pada tekanan konstan, didapatkan:

Hubungan antara kapasitas panas
Pengukuran kapasitas panas pada volume konstan seringkali sulit
dilakukan pada benda berwujud padat dan cair, karena perubahan
temperatur dapat membuat volume zat mengalami pemuaian sehingga
membutuhkan penampung yang memiliki kekuatan yang sangat tinggi. Lebih
mudah menghitung secara tekanan konstan dan lalu menurunkannya
menggunakan persamaan termodinamika dasar.

Bisa juga dituliskan dengan:

di mana
 adalah koefisien pemuaian
adalah koefisien pemuaian adalah kompresibilitas isotermal
adalah kompresibilitas isotermal
Rasio kapasitas panas atau
indeks adiabatik adalah rasio dari kapasitas panas pada tekanan konstan
terhadap kapasitas panas pada volume konstan, yang dapat disebut juga
sebagai faktor ekspansi isentropik.
Gas ideal
Untuk gas ideal, mengevaluasi persamaan turunan parsial di atas berdasarkan persamaan keadaan di mana R adalah konstanta gas ideal[1]



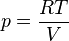 →
→ =
= 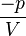
 →
→
Substitusikan
 =
= 
Sehingga akan didapatkan persamaan Mayer jika direduksi

Kapasitas panas spesifik (panas jenis)
Kapasitas panas spesifik (atau panas jenis) adalah kapasitas panas per basis massa

di mana pada ketiadaan transisi fase zat akan didapatkan panas jenis:

di mana
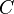 adalah kapasitas panas
adalah kapasitas panas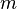 adalah massa zat
adalah massa zat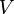 volume zat
volume zat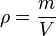 massa jenis zat
massa jenis zat
Untuk gas dan bahan lainnya yang berada pada tekanan tinggi, terdapat
perbedaan nilai panas jenis pada kondisi yang berbeda. Kapasitas panas
dapati didefinisikan dengan measukkan kondisi proses isobarik (tekanan konstan,  ) danproses isokhorik (volume konstan,
) danproses isokhorik (volume konstan,  ). Hubungan panas jenisnya dapat dirumuskan dengan:
). Hubungan panas jenisnya dapat dirumuskan dengan:
 ) danproses isokhorik (volume konstan,
) danproses isokhorik (volume konstan,  ). Hubungan panas jenisnya dapat dirumuskan dengan:
). Hubungan panas jenisnya dapat dirumuskan dengan:

Sesuai dengan persamaan sebelumnya:








0 komentar:
Posting Komentar